腫瘤相關(guān)超級(jí)增強(qiáng)子的研究方案及其在細(xì)胞技術(shù)研發(fā)中的應(yīng)用前景
引言
超級(jí)增強(qiáng)子是基因組上一類由多個(gè)相鄰的典型增強(qiáng)子簇集而成的、具有超強(qiáng)轉(zhuǎn)錄激活能力的順式調(diào)控元件。近年來(lái)的研究發(fā)現(xiàn),超級(jí)增強(qiáng)子在維持細(xì)胞身份、調(diào)控發(fā)育過(guò)程以及驅(qū)動(dòng)多種疾病,尤其是腫瘤的發(fā)生發(fā)展中起著關(guān)鍵作用。腫瘤相關(guān)超級(jí)增強(qiáng)子(Tumor-Associated Super-Enhancers, TASEs)的異常激活或形成,是驅(qū)動(dòng)癌基因高表達(dá)、促進(jìn)腫瘤細(xì)胞增殖、侵襲和轉(zhuǎn)移的重要機(jī)制。因此,深入解析TASEs,不僅有助于揭示腫瘤發(fā)生的新機(jī)制,也為基于細(xì)胞技術(shù)的腫瘤診斷和治療策略研發(fā)提供了極具潛力的新靶點(diǎn)和新方向。
一、腫瘤相關(guān)超級(jí)增強(qiáng)子的核心研究方案
針對(duì)TASEs的系統(tǒng)性研究,通常遵循一套多層次、多技術(shù)整合的方案。
- 鑒定與圖譜繪制:
- 技術(shù)手段:主要利用染色質(zhì)免疫沉淀測(cè)序(ChIP-seq),針對(duì)組蛋白修飾標(biāo)記(如H3K27ac)、轉(zhuǎn)錄因子(如MED1、BRD4)以及染色質(zhì)可及性測(cè)序(ATAC-seq)等技術(shù),在全基因組范圍內(nèi)鑒定和繪制不同腫瘤類型及細(xì)胞系中的超級(jí)增強(qiáng)子圖譜。
- 分析重點(diǎn):通過(guò)生物信息學(xué)分析,比較腫瘤組織與正常組織、不同亞型腫瘤、或治療前后樣本中超級(jí)增強(qiáng)子的差異,鎖定與腫瘤發(fā)生發(fā)展特異性相關(guān)的TASEs。
- 功能驗(yàn)證與機(jī)制解析:
- 基因編輯技術(shù):利用CRISPR/Cas9系統(tǒng)對(duì)候選TASEs進(jìn)行定點(diǎn)刪除(deletion)或干擾(干擾其結(jié)合蛋白,如使用dCas9-KRAB進(jìn)行抑制),隨后通過(guò)RNA-seq、細(xì)胞增殖、凋亡、侵襲遷移等實(shí)驗(yàn),在細(xì)胞和動(dòng)物模型中驗(yàn)證其對(duì)下游靶基因表達(dá)及腫瘤表型的調(diào)控功能。
- 染色質(zhì)構(gòu)象分析:采用染色質(zhì)構(gòu)象捕獲技術(shù)(如Hi-C、ChIA-PET)揭示TASEs與其靶基因啟動(dòng)子之間的三維空間互作,確認(rèn)其直接的調(diào)控關(guān)系。
- 關(guān)鍵因子挖掘:通過(guò)質(zhì)譜分析、蛋白質(zhì)相互作用研究等手段,鑒定驅(qū)動(dòng)和維持特定TASEs活性的關(guān)鍵轉(zhuǎn)錄因子、輔因子和表觀遺傳閱讀器。
- 臨床關(guān)聯(lián)與轉(zhuǎn)化研究:
- 分析TASEs的活性或靶基因表達(dá)水平與患者臨床病理特征(分期、分級(jí)、預(yù)后)的相關(guān)性,評(píng)估其作為生物標(biāo)志物的潛力。
- 探索靶向TASEs或其關(guān)鍵組分的小分子抑制劑(如BET抑制劑、CDK7/9抑制劑)在臨床前模型中的療效,為藥物研發(fā)提供依據(jù)。
二、在細(xì)胞技術(shù)研發(fā)與應(yīng)用中的廣闊前景
對(duì)TASEs的深入理解,正直接推動(dòng)著腫瘤領(lǐng)域細(xì)胞技術(shù)的革新。
- 新型細(xì)胞模型構(gòu)建:
- 利用對(duì)TASEs的操控,可以在正常細(xì)胞中“安裝”特定的致癌TASEs,或在腫瘤細(xì)胞中“關(guān)閉”關(guān)鍵TASEs,從而構(gòu)建出能更精準(zhǔn)模擬腫瘤發(fā)生、演進(jìn)或去分化/再分化過(guò)程的體外細(xì)胞模型。這些模型對(duì)于藥物篩選和機(jī)制研究具有更高保真度。
- 細(xì)胞治療策略的優(yōu)化:
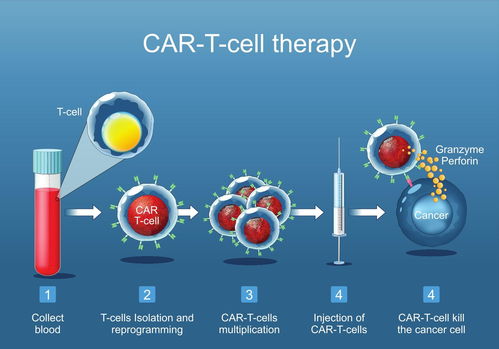
- CAR-T/TCR-T細(xì)胞療法:TASEs研究有助于發(fā)現(xiàn)僅在腫瘤細(xì)胞中高表達(dá)、且對(duì)腫瘤存活至關(guān)重要的新抗原(由TASEs驅(qū)動(dòng)的基因編碼)。這些抗原是設(shè)計(jì)下一代高特異性、低脫靶毒性CAR-T或TCR-T細(xì)胞的理想靶點(diǎn)。
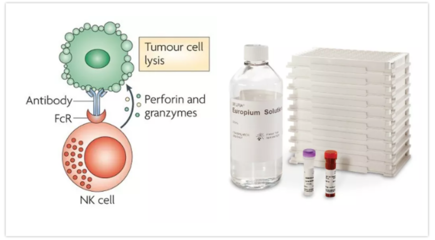
- 免疫細(xì)胞功能增強(qiáng):研究免疫細(xì)胞(如T細(xì)胞、NK細(xì)胞)自身的超級(jí)增強(qiáng)子網(wǎng)絡(luò),可以通過(guò)基因編輯或表觀遺傳藥物定向增強(qiáng)其抗癌相關(guān)基因(如細(xì)胞因子、效應(yīng)分子)的表達(dá),從而打造“超級(jí)免疫細(xì)胞”,提高過(guò)繼性細(xì)胞治療的持久性和效力。
- 基于細(xì)胞的精準(zhǔn)診斷與預(yù)后判斷:
- 從患者體液(如血液、胸腔積液)中分離的循環(huán)腫瘤細(xì)胞(CTCs)或外泌體中,檢測(cè)特定TASEs的活性標(biāo)志,可作為一種微創(chuàng)的“液體活檢”手段,用于腫瘤的早期診斷、分子分型、微小殘留病灶監(jiān)測(cè)及療效動(dòng)態(tài)評(píng)估。
- 細(xì)胞重編程與再生醫(yī)學(xué)中的風(fēng)險(xiǎn)控制:
- 在誘導(dǎo)多能干細(xì)胞(iPSC)技術(shù)或直接細(xì)胞轉(zhuǎn)分化中,對(duì)重編程過(guò)程中異常激活的、可能致癌的超級(jí)增強(qiáng)子進(jìn)行監(jiān)測(cè)和干預(yù),有助于提高生成細(xì)胞的安全性,降低成瘤風(fēng)險(xiǎn),推動(dòng)其向臨床安全轉(zhuǎn)化。
結(jié)論與展望
腫瘤相關(guān)超級(jí)增強(qiáng)子研究,架起了基礎(chǔ)腫瘤生物學(xué)與前沿細(xì)胞技術(shù)應(yīng)用之間的橋梁。通過(guò)系統(tǒng)性的研究方案,我們正不斷揭示TASEs在腫瘤中的奧秘。而其應(yīng)用前景,已深度滲透到從疾病模型構(gòu)建、新型細(xì)胞療法開發(fā)、到精準(zhǔn)診斷的整個(gè)鏈條。隨著單細(xì)胞多組學(xué)技術(shù)、高分辨率空間轉(zhuǎn)錄組學(xué)以及更高效的基因編輯工具的進(jìn)步,對(duì)TASEs的動(dòng)態(tài)調(diào)控和細(xì)胞異質(zhì)性作用的理解將更加深入。在此基礎(chǔ)上,發(fā)展出特異性靶向致病TASEs而不過(guò)度干擾正常細(xì)胞基因組的“表觀遺傳精準(zhǔn)醫(yī)療”策略,以及與細(xì)胞技術(shù)深度融合的個(gè)體化治療方案,將成為戰(zhàn)勝腫瘤的重要新武器。
如若轉(zhuǎn)載,請(qǐng)注明出處:http://www.brand100.cn/product/24.html
更新時(shí)間:2026-04-26 20:15:19